5. 기대가 컸던 만큼 아쉬움이 컸던 후보: IDO 저해제
PD-1/PD-L1 이후 가장 기대를 모았던 표적은 IDO였다.
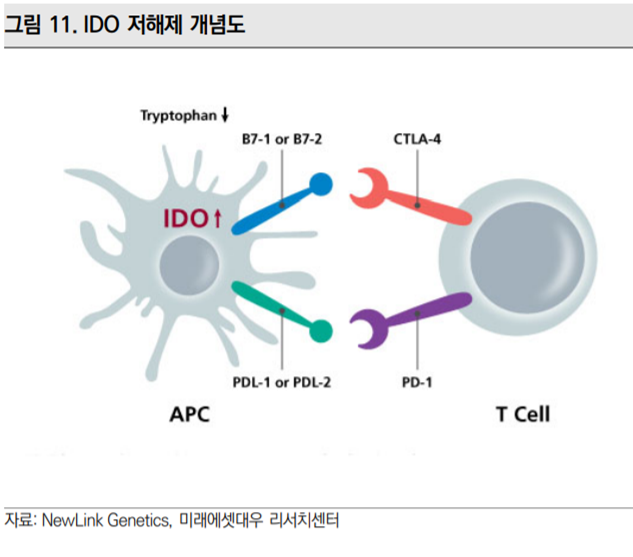
IDO는 필수 아미노산인 트립토판을 분해해 면역세포의 활성을 억제하는 단백질이다. BMS와 로슈, 화이자 등 다국적 제약사가 바이오텍 으로부터 후보물질을 도입했고 PD-1 저해제와 병용투여시 초기 임상 결과가 고무적이었다.
하지만 결국 개발에 실패했다. 대표적인 실패 사례는 인사이트의 에파카도스타트다.
IDO 저해제 중 가장 큰 규모로 임상3상을 진행했고, ASCO 2017에서 폐암 및 신장암 환자 대상 의미 있는 임상 결과를 발표했으며, 머크와 BMS, 아스트라제네카와 협력 관계에 있었다. 당시 에파카도스타트의 예상 매출액은 2조원을 상회 했었으나, 18년 4월 흑색종 환자 대상 임상3상의 1차 평가지표인 OS(전체 생존기간)와 PFS(무진 행 생존기간)를 충족하지 못해 개발을 중단했다. 당일 인사이트의 주가는 23% 폭락했다.
BMS도 플렉서스 바이오사이언시스를 12.5억 달러 규모로 인수해 흑색종과 폐암, 두경부암을 대상으로 옵디보와 병용 임상3상을 진행했지만 중단했고, 로슈와 화이자도 각각 뉴링크 제네틱스와 아이테오스 테라퓨틱스에서 도입한 IDO 저해제의 개발을 중단했다. 릴리도 올해 초 파이프라인 리스트에서 IDO 후보물질을 제외했기에 IDO 저해제에 대한 기대는 크게 낮아진 상황이다.

6. IDO 저해제 뒤를 이을 다음 선수는?
이제 업계의 관심은 IDO 저해제에서 LAG-3와 TIM-3, TIGIT, VISTA, B7-H3 저해제 등으로 옮 겨왔다. 리간드/리셉터의 상호 작용도 서서히 밝혀지고 있으며, 임상시험을 통해 그 가능성이 입증 되고 있다. 다른 면역항암제와 병용투여 시 시너지 효과가 나타난다는 점도 확인됐기에 ‘Next 키트루다’의 가능성은 높아지고 있다.

6.1. 첫 번째 후보: LAG-3 저해제
LAG-3는 CD223으로도 알려져 있으며 활성화된 도움T세포와 세포독성T세포, 조절T세포, 일부 NK세포, B세포 등에서 발현된다. 주요 리간드는 MHC-II(Major histocompatibility complex, 주 조직적합성 복합체)다.
PD-1과 마찬가지로 T세포의 활성화와 사이토카인을 억제하는 역할을 하며, 암세포가 분화할 때 면역 감시를 피하기 위해 LAG-3 경로를 이용한다. 따라서 LAG-3를 저해하면 면역세포가 활성화 되고 암세포의 성장이 억제될 것으로 예상하며, 특히 PD-1 내성을 지연시키거나 극복할 수 있을 것으로 기대된다.

가장 먼저 개발된 LAG-3 저해제는 이뮤텝의 IMP321(Eftilagimod alpha)이다.
단독요법으로는 효능이 미미했기에 PD-1 저해제 또는 저분자화합물과 병용요법으로 비소세포폐암, 두경부암, 전 이성 유방암, 고형암 등을 대상으로 임상을 진행하고 있다.
비소세포폐암, 두경부암은 머크와, 고형 암은 화이자와 공동 개발 중이다.

현재까지 발표된 임상 결과를 보면 LAG-3 저해제의 효능은 명확해 보인다. 17명 대상이긴 하지만 비소세포폐암 1차 치료제로의 키트루다 병용 데이터를 보면, 객관적반응률(ORR) 52.9%, 질병통 제율(DCR) 82.4%를 기록했다. 키트루다 단독의 경우 객관적반응률이 20% 이하, 여보이+옵디보 병용요법이 33%, 키트루다+화학항암제 병용요법이 48%임을 감안하면 시너지 효과는 크다고 판단한다.

18명 대상으로 한 두경부암 2차 치료제로의 데이터도 기존 치료법 대비 우수한 반응률을 기록했 다. 키트루다와 IMP321을 병용투여했을 때 객관적반응률 33.3%와 질병통제율 50.0%를 기록했 는데, 이는 키트루다 단독의 객관적반응률 14.6%를 두 배 이상 높인 수준이다.

임상 단계가 가장 앞선 LAG-3 저해제는 BMS의 렐라틀리맙(BMS-986016)이다.
LAG-3 저해제 중 유일하게 임상3상에 진입했으며, 적응증은 흑색종이다. 렐라틀리맙+옵디보 병용투여 임상1/2a상에서 평가 가능한 흑색종 환자 48명 중 객관적반응률은 12.5%였다. LAG-3 발현이 1% 이상인 환자의 객관적반응률은 20%로 발현이 1% 미만인 환자 의 객관적반응률 7.1%보다 높았으며, 여보이+옵디보 병용 대비 안전성이 우수했다.
여기서 주목해야 할 부분은 48명 모두 면역항암제가 듣지 않는 환자였으며, 이중 47%는 3번 이 상 다른 치료를 받은 경험이 있는 환자라는 점이다. 따라서 면역항암제 불응성 환자 대상으로 상업 화를 기대해 볼 수 있다.
이 밖에 머크의 MK-4280이 비소세포폐암 대상 임상2상 중이며, 베링거인겔하임과 로슈, 리제네 론의 LAG-3 저해제도 임상1상에 진입했다. 국내에서는 와이바이오로직스가 LAG-3 항체 YBL-011을 개발해 전임상 중에 있으며, 에이비엘 바이오는 PD-L1과 LAG-3를 동시에 저해하는 이중항체 ABL501을 개발 중이다.

To-be Continue...
출처: 미래에셋대우증권, Global Data, Immutep, Medical Graphics, Molecular Cancer, Newlink Genetics
뜨리스땅
구독과 공감, 댓글은 힘이 됩니다.
'바이오, 의학, 제약' 카테고리의 다른 글
| 바이오 기술 탐구: 면역항암제 4(feat. 메드팩토, 제넥신) (0) | 2020.09.04 |
|---|---|
| 바이오 기술 탐구: 면역항암제 3(feat. 메드팩토) (0) | 2020.09.02 |
| 바이오 기술 탐구: 면역항암제 1(feat. 메드팩토) (0) | 2020.09.02 |
| 바이오 기업 탐구: 메드팩토 (0) | 2020.08.27 |
| 바이오 기업 탐구: 제넥신(Genexine) 2 (2) | 2020.08.01 |




댓글